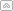При окислении С., содержащих d-H-атом, происходит циклизация с образованием производных фурана, напр.: При взаимод. С2Н5ОН с гипогалогенитами Na образуются соотв. хлороформ, бромоформ и йодоформ (т. наз.
галоформная р-ция):
Анализ. С. дают окрашенные соед. с соед. Ce(IV), напр. аммонийцерийгексанитратом (NH4)2 [Ce(NO3)6]. Для
идентификации С. используют р-ции с хлорангидридами бензойной или 3,5-динитробензойной к-ты, либо с
фенил-изоцианатом, приводящие к образованию хорошо кристаллизующихся эфиров бензойной к-ты или уретанов.
Для количеств. определения гидроксильных групп применяют метод Церевитинова: ROH + R'MgX : ROMgX + R'H,
a для смесей используют хроматографич. методы.
Получение. Получают С. гидратацией олефинов и присут. H2SO4 или Н3РО4 (в осн. алканолы С2-С4);
восстановлением СО на катализаторах Zn-Сг при т-ре 300-400 °С и давлении 25-45 МПа (наряду с СН,ОН образуются
С3Н7ОН, изо-С4Н9ОН и алканолы С5-С14); гидролизом галогенсодержащих соед.; взаимод. карбонильных соед. с
реактивами Гриньяра, напр.:
Для получения С. используют также восстановление карбонильных соед. натрием, его амальгамой, LiAlH4 в условиях
р-ции Меервейна-Понндорфа-Верлея, гидрирование в присут. катализаторов (Pt, Ni) либо электролитич.
восстановление.
Для пром. получения бутанола, 2-этилгексанола и пента-эритрита используют альдольную конденсацию, напр.:
Первичные С. (в т. ч. ароматические) образуются по р-ции Канниццаро либо при взаимод. бензола с алкеноксидами в
присут. АlСl3 в условиях р-ции Фриделя-Крафтса; ацетиленовые-по р-ции Реппе; гидроксиэфиры-в условиях р-ции
Кнёвенагеля, напр.:
Известны др. способы синтеза С.: гидроборирование ал-кенов, гидролиз сложных эфиров, ферментативное брожение
Сахаров.
Применение. Применяют С. как полупродукты в синтезе разл. орг. соед. (формальдегида, ацетальдегида, ацетона,
уксусной к-ты, диэтилового эфира, сложных эфиров карбо-новых к-т), в произ-ве красителей, синтетич. волокон,
душистых в-в, лек. препаратов, моющих ср-в, пластификаторов и мономеров, в пищ. пром-сти. С. используют как
р-рители, ПАВ и др., метиловый спирт также в качестве моторного топлива.
Наиб. значение имеют амиловые спирты, бензиловый спирт, бутиловые спирты, высшие жирные спирты,
метиловый спирт, пентаэритрит, пропиловый спирт, b-фенил-этиловый спирт, циклогексанол, этиленгликоль,
этиловый спирт.
Среди С. наиб. токсическим действием обладает метанол (смертельная доза 100-150 мл), окисляющийся в организме
до формальдегида и муравьиной к-ты. Токсичность многоатомных спиртов невысока, за исключением
эти-ленгликоля, образующего в организме ядовитую щавелевую к-ту.